Uma equipa de investigadores do Instituto de Investigação e Inovação em Saúde da U.Porto (i3S) acaba de publicar na prestigiada revista científica Cell Reports um estudo que evidencia uma interação – entre a notocorda e o primórdio pancreático do embrião – fundamental para o correto desenvolvimento do pâncreas.
O trabalho explica pela primeira vez o mecanismo que regula a formação deste órgão e revela pistas que poderão ser úteis ao cultivo de células pancreáticas produtoras de insulina, essenciais para terapias regenerativas em doentes com diabetes.
O pâncreas é um órgão vital, tanto no controlo dos níveis de glicose no sangue, através da produção de insulina pelas células beta, como na secreção de enzimas digestivas que ajudam a regular o sistema digestivo. O mau funcionamento do pâncreas pode resultar em várias doenças, entre elas, a diabetes.
O “segredo” está na notocorda
O pâncreas surge no embrião a partir de um grupo de células progenitoras, sob o controlo de vias de sinalização geradas na notocorda (estrutura em forma de bastão, flexível com um aspecto cartilaginoso, na região dorsal dos embriões organismos, designados cordados, e que mantém na fase adulta de alguns), que ajudam a determinar a sua correta posição e tamanho.
“Um trabalho nos anos 90, com embriões de galinhas, tinha deixado claro que a notocorda era essencial para a formação do pâncreas, pois quando os investigadores a retiravam o pâncreas não se desenvolvia; mas as moléculas envolvidas nessa comunicação é algo que ainda não havia sido esclarecido”, destaca José Bessa, líder do grupo «Vertebrate Development and Regeneration» do i3S e coordenador do estudo agora publicado.
Já João Amorim, primeiro autor do artigo, explica que a equipa identificou, precisamente, “a proteína que é expressa na notocorda e que serve de sinalização à formação do pâncreas no embrião de peixe-zebra”, denominada Nog2. No trabalho, os investigadores mostraram que “a Nog2 funciona como potenciador específico do tecido que dará origem ao pâncreas; ela é produzida na notocorda e difunde-se para a região progenitora pancreática, controlando o tamanho do pâncreas”.

João Amorim é p primeiro autor do artigo que identifica uma proteína essencial para a formação do pâncreas em embriões de peixe-zebra. (Foto: i3S)
Ao induzirem a perda de função da Nog2, os investigadores observaram a redução do número de células progenitoras do pâncreas e também das células produtoras de insulina. Contudo, mantinha-se em aberto uma questão importante: qual o local, na sequência do genoma, que controla a expressão da própria Nog2 na notocorda?
Para responder a esta questão, os investigadores do i3S procuraram em regiões de DNA do peixe-zebra, próximas do gene que codifica a Nog2, padrões de atividade associados a regiões controladoras da expressão génica, tendo identificado várias sequências candidatas. Silenciando uma a uma, identificaram a sequência responsável pela expressão desta proteína na notocorda. Ao deletarem essa sequência os investigadores induziam, de forma similar, uma redução do número de células pancreáticas, por redução da expressão da Nog2.
Dos peixe para os humanos
Este mecanismo de regulação da Nog2 na notocorda em peixe-zebra já foi comparado com elementos reguladores humanos na mesma fase. Embora as sequências dos elementos de regulação sejam distintas nos dois organismos, foi possível identificar as sequências que, por comparação de atividade, cumpriam a mesma função em humanos.
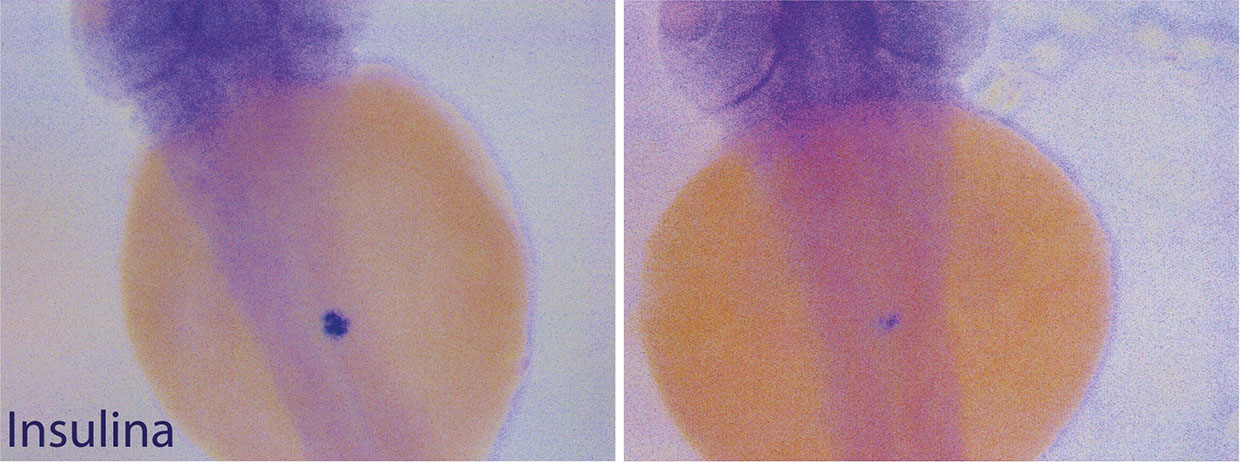
Embriões de peixe zebra, com pâncreas normal e subdesenvolvido.
A existência de anomalias raras, de humanos com pâncreas subdesenvolvidos, permitiu estabelecer a correlação final, sugerindo a existência de mecanismos fundamentais para a formação do pâncreas, equivalentes ao longo de várias linhagens de vertebrados.
Note-se que o tratamento da diabetes tem tido muitas abordagens. Entre as mais promissoras está o cultivo e diferenciação in vitro de células produtoras de insulina. Como os mecanismos que controlam essa diferenciação não são conhecidos, esta descoberta será fundamental para melhorar os meios e condições que favorecem a produção dessas células.